背景介绍
Smads家族蛋白在将TGF-β信号从细胞表面受体传导至细胞核的过程中起到关键性作用,且不同的Smad介导不同的TGF-β家族成员的信号转导。TGF-β作为配体形成的受体复合物,激活Smads进入核内,共同激活或抑制它们调节的靶基因的转录。
Smads家族
脊椎动物中目前发现的Smads蛋白至少有9种,根据结构和功能,Smads家族蛋白可分为三类(图1):
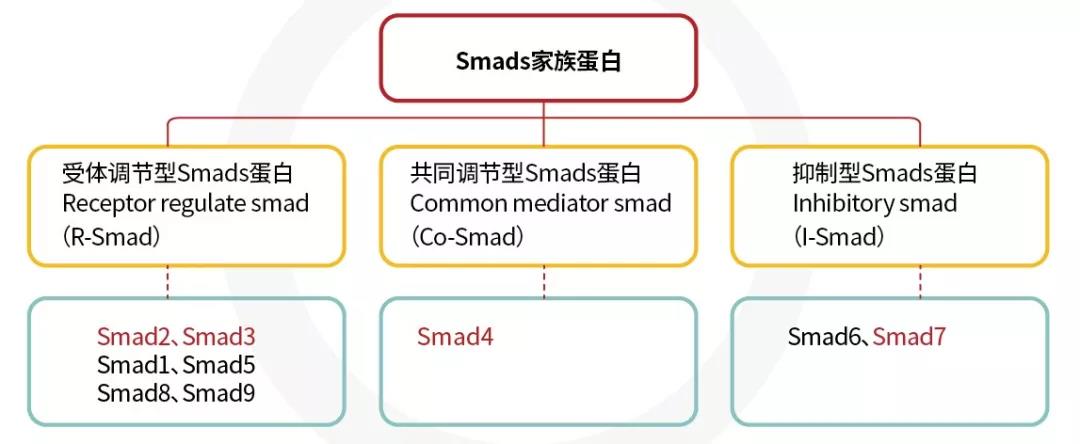
图1:红色标记的为参与TGF-β信号转导的Smad蛋白
1、TGF-β细胞信号转导
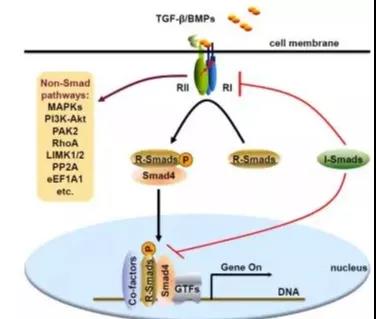
TGF-β细胞信号转导在不同的层面受到精细的调控,包括配体、受体、Smads家族蛋白以及核内转录水平的调控;其调控机制多种多样,比如蛋白-蛋白相互作用、蛋白翻译后修饰、蛋白降解、蛋白运输与细胞内定位,以及Smad-DNA结合等。几乎所有的组织细胞都含有TGF-β受体。目前已知的TGF-β受体分为三种类型:I型(RI)、II型(RII)和III型(RIII),其中RI和RII参与信号转导。由于RI可以激活Smads家族蛋白,但不能与TGF-β直接结合, RII虽然可以与TGF-β结合,却不能激活Smads家族蛋白,所以只有RI和RII在细胞膜上共同表达的情况下,才能使胞外信号转导至细胞内。简单来讲,RII与TGF-β结合被活化,活化的RII募集并结合RI形成RII-配体-RI异源三聚体,激活RI胞内结构域中的GS区,活化的RI继续磷酸化Smads家族蛋白,从而将信号转导至细胞内(图2)。TGF-β信号转导异常则可能导致多种疾病的发生,比如胚胎发育异常、肿瘤、组织纤维化、心血管疾病和免疫性疾病等。
2、Smads家族蛋白作用机制
Smads家族蛋白活化
Smads家族蛋白的活性受到多种激酶的调控。R-Smads的linker区富含丝氨酸与苏氨酸,其中很多位点都是脯氨酸导向激酶的靶点。其中,Smad2和Smad3参与TGF-β/活化素信号通路,而Smad1、Smad5和Smad9调节BMP(骨形态发生蛋白)信号通路。Smads的羧基端被活化受体磷酸化后导致其与常见信号转导因子 Smad4 结合,并转运入胞核。激活的Smads可通过与转录因子结合,调节各种不同的生物学效应,导致细胞状态特异性转录调节。由于I-Smads和R-Smads结构相似,而且I-Smads能更有效的结合RI,所以 Smad6和Smad7可拮抗R-Smads的激活。Smad6和Smad7的表达由活化素/TGF-β和BMP信号转导一起诱导,并作为负反馈回路的一部分。Smad7是TGF-β家族的广谱抑制蛋白,而Smad6更特异性的抑制BMP信号。
3、Smads家族蛋白稳定性调控
Smads家族蛋白除了可以被磷酸化修饰以发挥作用外还可以进行其他的翻译后修饰以发挥相应功能。例如Smurf E3 泛素连接酶和 USP4/11/15 去泛素化酶共同调节Smads家族蛋白的稳定性。Co-Smad/Smad4的蛋白稳定性也受E3泛素连接酶的控制,Smad蛋白的磷酸化修饰经常与泛素化降解相偶联,从而协同调控Smad的活性与命运。另外,乙酰转移酶p300、CBP和PCAF能够在体内乙酰化Smad2/3,并通过抑制Smad2出核或者促进Smad3和Smad2与DNA的结合能力等途径增强Smad的转录活性。
4、Smads家族蛋白的核质穿梭
Smads家族蛋白的核质穿梭在信号沉默阶段和信号转导阶段均可发生,对于TGF-β信号转导十分重要。信号沉默阶段,R-Smads主要定位于细胞质,Smad4在胞质和胞核均有定位。R-Smads MH1结构域有一个富含赖氨酸的H2螺旋,在Smad1和Smad3中起核定位信号(NLS)的作用。信号转导阶段,C末端磷酸化使Smad1和Smad3构型改变,NLS暴露,与β-importin(输入蛋白)结合入核,Smad4与α-importin结合入核。Smad2入核由MH2结构域介导,需要MH2与核膜蛋白CAN/Nup214和Nup153相互竞争作用,Nup214的过表达可抑制Smad2的核内聚集。尽管在Smad1/2/3和Smad4中都含有出核信号(NES),但它们出核的分子机制却不一样。Smad1/4通过exportin 1/CRM1转运出核;而Smad3则由exportin 4介导出核;此外,另一个exportin家族成员RanBP3也能将Smad2/3转运至细胞质中。Smads家族蛋白的核质穿梭有利于它们感受受体的活性,从而决定信号的强度与持续性。
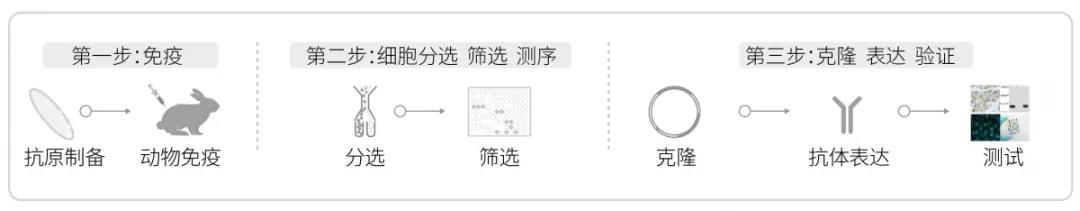
图3:ABclonal第四代重组兔单抗制备流程
ABclonal第四代重组兔单克隆抗体制备采用创新的细胞分选、富集、生物信息学和重组单克隆抗体技术,直接从B细胞中获得理想的兔单克隆抗体。ABclonal在加强自身抗体升级的同时,也可对外承接兔单抗定制服务。
案例展示
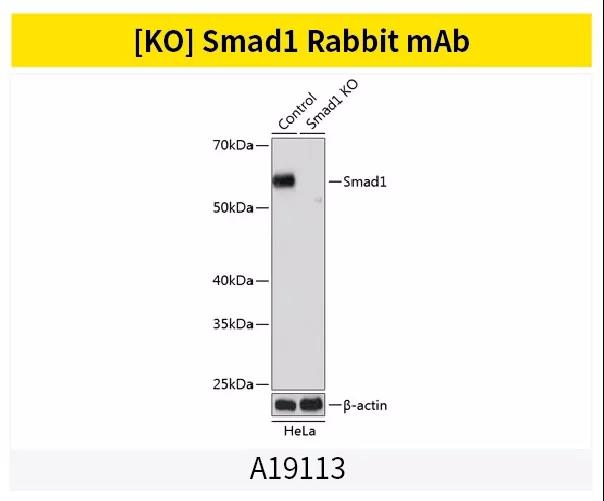
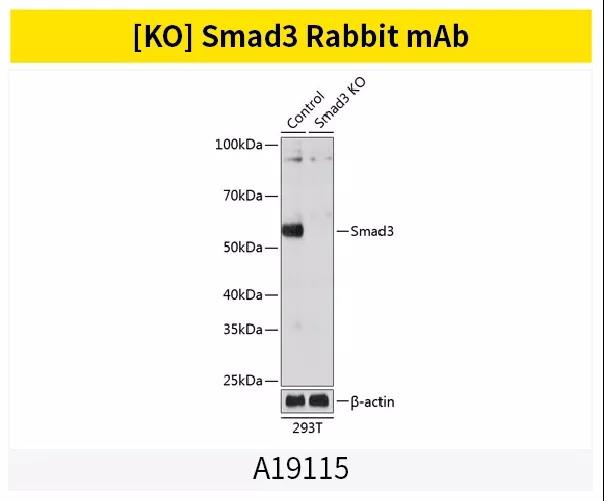
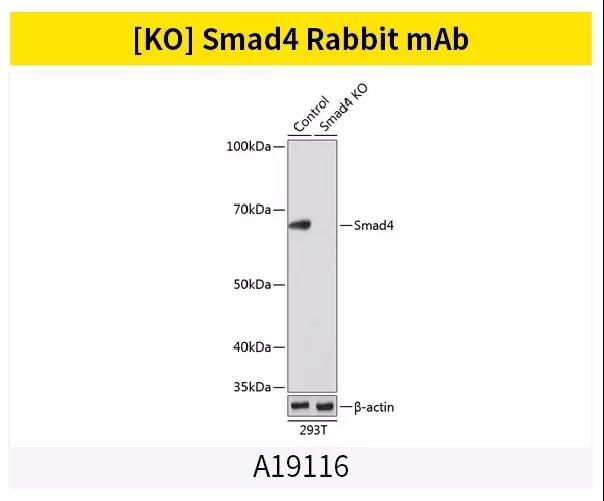
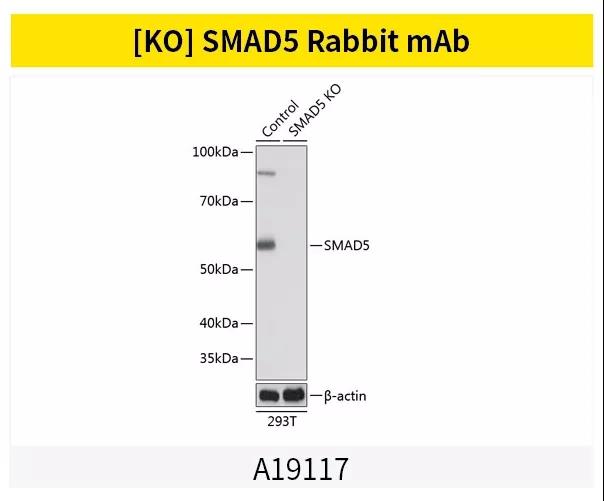
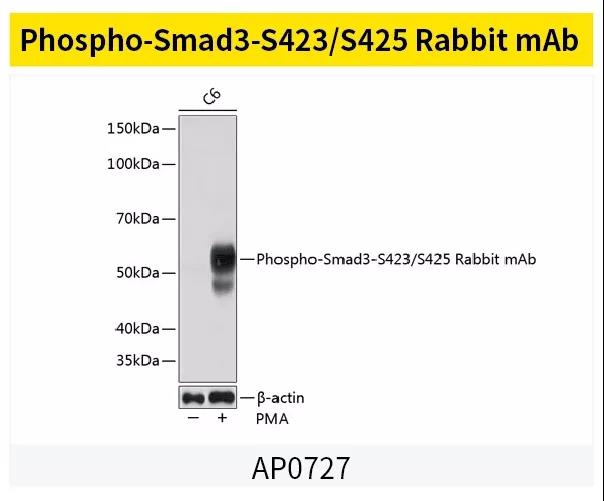
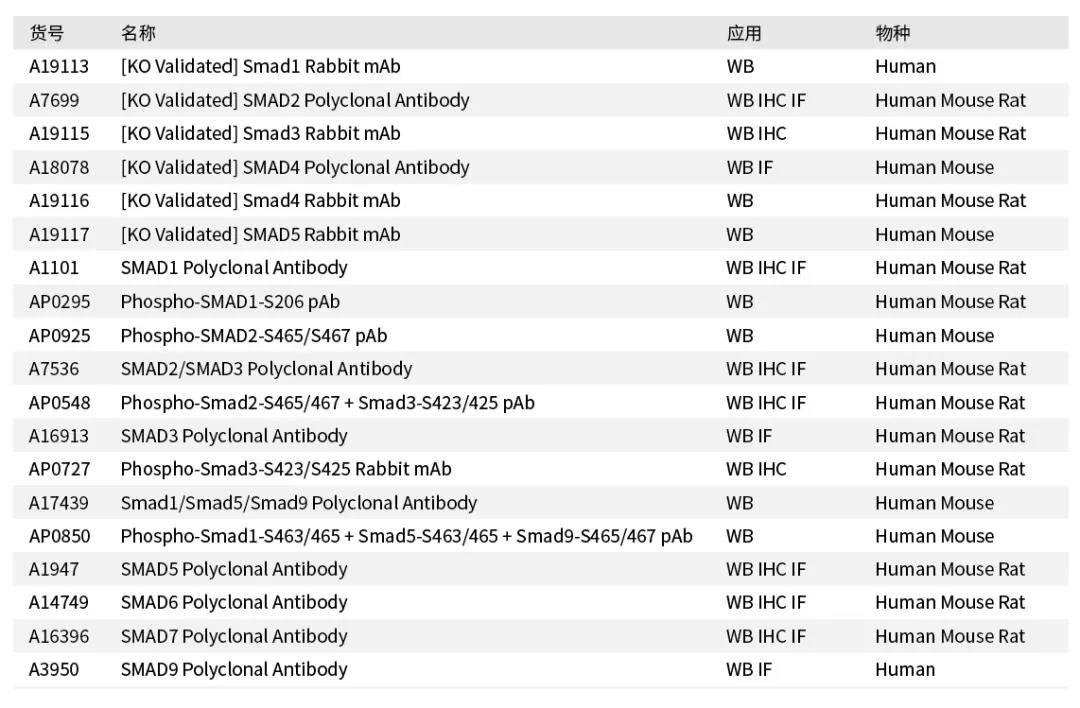
Smads家族蛋白相关抗体